La teoria prevalente, formulata alla metà del secolo scorso, interpreta il cancro come un insieme di circa 200 malattie, caratterizzate da un’abnorme crescita cellulare, svincolata dai normali meccanismi di controllo dell’organismo.
Come sta cambiando lo scenario oncologico in Italia?
Ogni giorno circa 1.000 persone ricevono la diagnosi di tumore: è un numero importante che evidenzia il peso della patologia oncologica e lo sforzo continuo atto a migliorare la sopravvivenza dei pazienti non solo in termini quantitativi, ma anche in termini di qualità di vita.
Forse nemmeno in questo secolo il cancro sarà definitivamente sconfitto, ma di sicuro faremo molti progressi.
Oggi le due neoplasie più frequenti, il tumore della prostata negli uomini e quello della mammella nelle donne, presentano sopravvivenze a 5 anni di oltre il 90%, con percentuali ancora più elevate per i tumori diagnosticati in stadio precoce. Risultati sicuramente incoraggianti.
Se fino a qualche tempo fa si faceva solamente ricorso alla chirurgia per debellare e sconfiggere i piccoli tumori localizzati, oggi si raccontano successi su tumori molto più aggressivi, in stadio molto più avanzato, grazie a incoraggianti e brillanti strategie che in alcuni casi sono solo agli albori.
Ecco a che punto è la ricerca, partendo dagli strumenti più noti.
1. Chemioterapia e innovazioni
- Chemioterapia
Siamo nel 1943 al porto di Bari quando un bombardamento tedesco fece esplodere una nave americana che trasportava 70 tonnellate di iprite, altrimenti detta gas mostarda.
I primi a scoprire a loro spese gli effetti dell’iprite furono i marittimi del porto e gli abitanti delle zone più vicine.
Morirono un centinaio di persone per le orribili lesioni alla pelle e all’apparato respiratorio, ma soprattutto per la distruzione del midollo osseo e quindi delle cellule staminali dalle quali discendono le cellule del sangue.
Due ricercatori dell’università Yale, Louis Goodman e Alfred Gilman, studiando le cartelle cliniche dei soldati ipotizzarono che l’iprite potesse riuscire a distruggere anche i globuli bianchi maligni che si formano in alcune leucemie.
E un chimico inglese, Alexander Haddow, dimostrò che la molecola poteva essere resa ancora più tossica e creò l’azotoiprite, efficace contro i linfomi, tumori del linfonodi.
Era la prima chemioterapia, che ha dato origine ai cosiddetti “agenti alchilanti”, farmaci che uccidono le cellule tumorali in tumultuosa replicazione danneggiandone il Dna.
Sidney Farber, di Boston, dimostrò che uno di questi, l’aminopterina, induceva a remissione le leucemie acute infantili, bloccando una reazione chimica necessaria per la replicazione del Dna.
Era il progenitore del metotrexato, ancora in uso, capace di curare un raro tumore metastatico, il coriocarcinoma. Molti altri farmaci sono seguiti.
Nella foto la molecola dell'Iprite, o “gas mostarda”. - Innovazioni
Tuttavia, alla chemioterapia si stanno affiancando strategie farmacologiche che agiscono in modo diverso, e che di solito hanno meno effetti collaterali della chemio:
gli anticorpi monoclonali; le associazioni di due o più farmaci; nuove modalità di somministrazione, come quella attraverso i liposomi (vescicole che si fondono con la membrana delle cellule, rilasciando le molecole-farmaco che contengono).
E sono in via di diffusione anche farmaci che mirano a contrastare le conseguenze della chemioterapia:
fattori di stimolazione delle staminali; agenti chemioprotettivi come il dexrazoxano e l’amifostina; nuove molecole per ridurre nausea e vomito o per contrastare la perdita di capelli; farmaci capaci di agire quando il tumore non risponde più alle cure tradizionali.
Ma soprattutto, si lavora a terapie più mirate a seconda del tipo di cancro. Le più innovative agiscono influenzando i processi che controllano la crescita, la diffusione e la morte delle cellule tumorali. Con varie strategie:
1. bloccando i segnali di crescita, cioè la moltiplicazione delle cellule;
2. inibendo l’angiogenesi, cioè bloccando la crescita dei vasi sanguigni che permettono la vita delle cellule tumorali;
3. inducendo l'apoptosi cellulare, cioè spingendo la cellula al suicidio.
2. Immunoterapia
In particolare, i medici hanno imparato a utilizzare le risorse dell’organismo, capace in alcuni casi di eliminare da sé un tumore.
E la cosiddetta immunoterapia, scoperta oltre un secolo fa ma impiegata su larga scala solo a partire dagli anni Settanta.
Da allora, le sperimentazioni cliniche hanno dimostrato che vari tipi di immunoterapie, che modificano la risposta biologica, sono efficaci in molti tipi di tumore. Alcuni di questi agenti (molecole prodotte dal sistema immunitario) possono anche essere fabbricati in laboratorio.
Hanno nomi strani: interferoni, interleuchine, citochine... Ma tutti, somministrati ai pazienti, imitano e/o influenzano la normale risposta immunitaria che finisce per alterare la crescita tumorale oppure aiutano le cellule sane a contenere la diffusione del cancro.
E non è l’unica risorsa: sulle cellule tumorali sono state identificate particolari molecole, dette antigeni, che i ricercatori hanno utilizzato come bersaglio di proteine del sistema immunitario, gli anticorpi, prodotte in laboratorio con una tecnologia che risale ad alcuni decenni fa, detta “del Dna ricombinante”.
C’è voluto infatti un po’ di tempo: i primi anticorpi monoclonali terapeutici sono stati approvati alla fine degli anni Novanta. Si chiamano rituximab (Rituxan) e trastuzumab (Herceptin), utilizzati rispettivamente per la terapia del linfoma e del tumore al seno.
Ora gli anticorpi monoclonali fanno parte dell’armamentario comune dell’oncologo, ma molti altri, specifici per vari tipi di tumore, sono allo studio.
L’approccio di tipo immunitario è così promettente che i ricercatori studiano anche alcuni vaccini, capaci anch’essi di aumentare la risposta dell’organismo del paziente contro il tumore.
Nel 2010 l’agenzia del farmaco statunitense ha approvato la sperimentazione di sipuleucel-T (Provenge), un vaccino contro il tumore mestastatico della prostata diventato resistente ad altre terapie. Provenge ha prolungato la sopravvivenza di alcuni pazienti.
3. Il Micro-Rna
L’ultima arma contro i tumori sono però i cosiddetti “microRna” (miRna), piccoli spezzoni di materiale genetico simile al Dna.
Non contengono la ricetta per la fabbricazione di proteine, ma si legano all’Rna messaggero, cioè alla grossa molecola che porta l’istruzione genetica dal nucleo al resto della cellula tumorale, inibendone così il metabolismo interno.
Le cellule normali usano i miRna per aumentare il controllo temporale dell’accensione e dello spegnimento dell’attività dei geni.
Nelle cellule tumorali, queste molecole sembrano essere meno attive che nelle cellule sane, e alcuni miRna sono caratteristici delle cellule tumorali più aggressive.
Vengono quindi usati, per esempio, per riconoscere il tessuto del mesotelioma pleurico maligno (un tumore dovuto all’esposizione ad amianto), dal tessuto pleurico non canceroso.
I miRna potrebbero in futuro consentire quindi la diagnosi differenziale fra tumori aggressivi e forme tumorali che non richiedono intervento terapeutico, ma solo di essere tenute d’occhio, come alcune forme di tumore del polmone e del seno.
Oggi, però, si mira a usare i miRna anche come proiettili terapeutici: le mutazioni del gene umano chiamato Kras sono, per esempio, alla base di molti tumori del colon-retto e del polmone resistenti alla chemioterapia.
I ricercatori dell’University of California a San Diego hanno prodotto una grande varietà di miRna e ne hanno individuato uno, miR-1298, che inibisce due proteine (FAK e LAMB3) presenti nelle cellule tumorali, che a loro volta interferiscono con Kras, bloccando la crescita di questo tipo di cancro. Per ora in vitro.
Bisognerà verificare se tutto e ciò funziona anche in un organismo complesso come l'uomo. Del resto, il microRna è in sperimentazione anche per riparare i tessuti del cuore.
4. Cammino lungo
Nel 1896 un fisico tedesco, Wilhelm Conrad Röntgen, presentò a un congresso una relazione dal titolo “Su un nuovo tipo di raggi", che Wilhelm Röntgen chiamava raggi X.
Nel giro di pochi mesi, furono messi a punto sistemi in grado di usare i raggi X per la diagnosi (le radiografie), e negli anni successivi si pensò di usare le radiazioni per la cura del cancro.
Agli inizi del 1900, infatti, in Francia si scoprì che somministrando dosi quotidiane di radiazioni, nell’arco di molte settimane crescevano le possibilità di sopravvivenza dei pazienti.
I metodi e le macchine che somministrano la radioterapia da allora sono migliorati costantemente, e oggi si riescono a dirigere le radiazioni in modo molto preciso.
Ma la ricerca avanza anche in questo campo: recentemente sono entrate in uso sostanze che modificano chimicamente le cellule tumorali rendendole più sensibili alle radiazioni, in modo da poterne somministrare dosi relativamente basse, e così risparmiare i tessuti sani che circondano il tumore.
Anche se di novità terapeutiche antitumore ce ne sono, e tante, gli stessi medici consigliano comunque cautela.
Nel settembre scorso, a New York, durante la seconda conferenza internazionale sull'immunoterapia del cancro, Philip Greenber, ricercatore del Fred Hutchinson Cancer Research Center, dell’University of Washington, ha esortato:
«Siate critici, non credete a tutto quello che sentite». Certo, sono stati fatti "enormi" progressi nell'uso del sistema immunitario contro i tumori, ma non mancano le recidive e gli effetti collaterali. Vinay Prasad, onco-ematologo e docente dell'Oregon Health and Sciences University, tiene a ricordare che per ora solo il 30% dei pazienti con recidiva rispondonoa terapie con farmaci scelti in base ai marker biologici e che la sopravvivenza media libera dalla progressione del tumore è solo di 5,7 mesi. Insomma, le difficoltà dell’immunoterapia e della terapia di precisione sono le stesse di altre terapie inizialmente definite “rivoluzionarie".
Ma i progressi ci sono, un'altra fetta di pazienti guarisce e, nonostante le battute di arresto, nella comunità scientifica c'è ottimismo.
5. Come agiscono i farmaci
I medicinali capaci di contrastare la crescita dei tumori agiscono secondo tre strategie. Eccole:
- BLOCCO DEI SEGNALI DI CRESCITA
Tutte le cellule producono i cosiddetti “fattori di crescita”, molecole che inducono la cellula a moltiplicarsi, ma molte cellule tumorali ne fabbricano una forma modificata oppure quantità eccessive, a causa di mutazioni nei geni (oncogeni) dai quali parte l’informazione per produrli.
Ora esistono terapie che interferiscono con questi segnali, fermando la crescita cellulare. - INIBIZIONE DELL’ANGIOGENESI
L’angiogenesi è la creazione di nuovi vasi sanguigni. È un processo normale, utile anche nella riparazione di tessuti danneggiati.
Ma nei tumori questi rifornimenti di sangue servono a nutrirne le cellule. Il primo farmaco di questo tipo, il bevacizumab (Avastin) è in uso dal 2004 nella terapia del cancro del colon, del rene, e di altri tumori in stadio avanzato.
Altri farmaci antiangiogenetici sono in sperimentazione. - INDUZIONE DELL’APOPTOSI
L’apoptosi è un processo naturale grazie al quale le cellule danneggiate vengono indotte al suicidio. Anche la radioterapia e la chemioterapia agiscono danneggiando le cellule in modo irreparabile, sfruttando così il meccanismo dell’apoptosi.
Ma ci sono farmaci capaci di controllare direttamente la sopravvivenza della cellula o la sua morte.
Per esempio, i cosiddetti STING agonisti, molecole che inducono l’apoptosi nei linfociti B normali e maligni: farmaci che potrebbero curare alcune leucemie, linfomi e il mieloma multiplo.
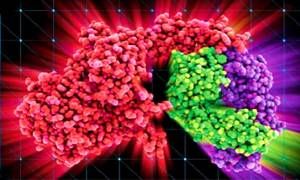
Nella foto l'azione di un anticorpo monoclonare (molecola verde e viola) sul recettore (in rosso) di una cellula tumorale.





